日本再生医疗风险等级划分
摘要
根据《再生医疗等安全性确保法》,日本将细胞治疗与再生医疗分为三种风险等级。本文全面解析第一种至第三种再生医疗的定义、适用范围与监管要求。
日本于2014年实施《再生医疗等的安全性确保等相关法律》(日文:再生医療等の安全性の確保等に関する法律),简称“再生医疗法”,旨在规范干细胞治疗、组织工程、基因治疗等再生医疗技术的临床应用。
法律依据与实施背景
- 法律名称:再生医療等の安全性の確保等に関する法律
- 公布时间:2013年11月27日
- 实施时间:2014年11月25日
- 主管机关:日本厚生劳动省
- 目的:在促进再生医疗发展的同时,确保患者安全,防止未经验证的治疗滥用。
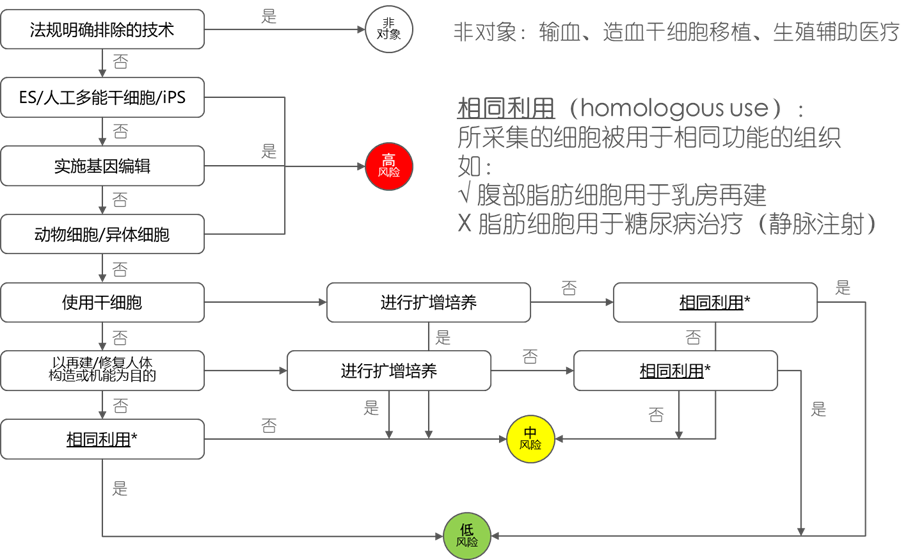
图1:日本再生医疗风险等级划分
再生医疗法将再生医疗分为三种等级,依据治疗对人体生命与健康的潜在影响程度,分别为:
第一种再生医疗(高风险)
- 定义:使用异体、异种等未经全行业充分验证的细胞等再生医疗制品种类,上市前需要经过严格验证、评审的评审。
- 典型例子:
- 使用诱导性多能干细胞(iPS细胞)或胚胎干细胞(ES细胞)进行治疗
- 基因改造细胞治疗
- 监管要求:
- 必须提交“第一种再生医疗提供计划”给厚生劳动大臣
- 需经特定认可再生医疗等委员会审查
- 实施前需接受厚生劳动省组织的科学审议会审评,并设有实施限制期以观察安全性
第二种再生医疗(中风险)
- 定义:使用自体细胞,需要体外扩增等人工加工,治疗方法尚未广泛验证,存在一定风险。
- 典型例子:
- 自体脂肪干细胞注射治疗关节等疾病
- 自体骨髓间充质干细胞移植治疗神经系统等疾病
- 监管要求:
- 提交“第二种再生医疗提供计划”
- 需经特定认可再生医疗等委员会审查
- 原则上不需厚生劳动省批准,但需备案
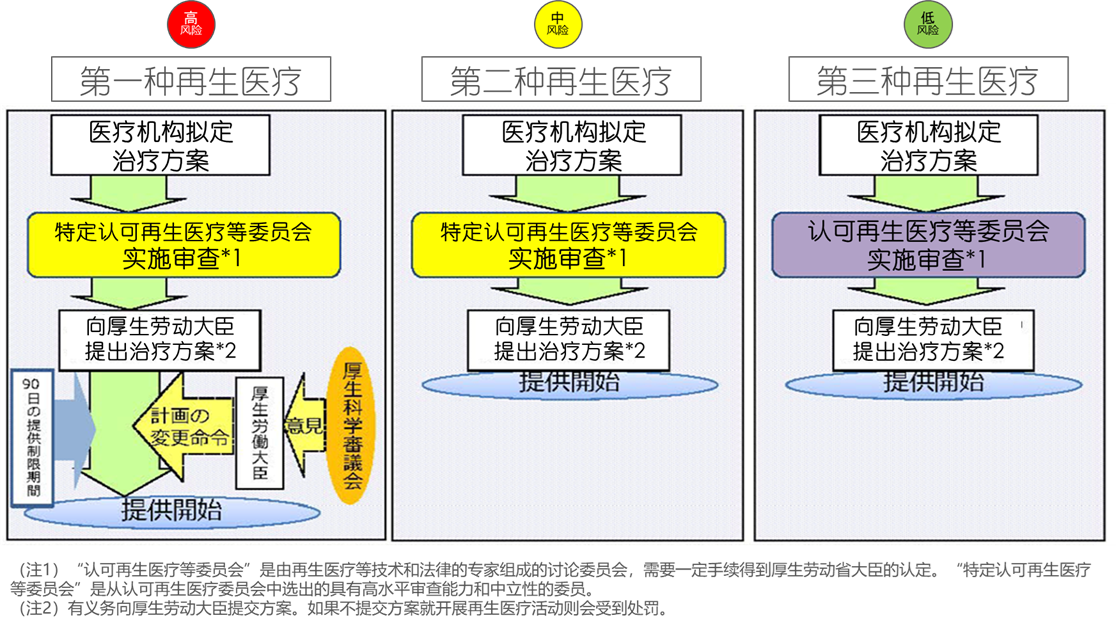
图2:日本再生医疗审批分类
第三种再生医疗(低风险)
- 定义:使用自体细胞,使用浓缩等相对简单的体外加工,治疗方法一定程度被广泛使用,风险较低。
- 典型例子:
- 自体血液中提取的富血小板血浆(PRP)提取与注射
- 自体免疫细胞移植用于癌症预防治疗
- 监管要求:
- 提交“第三种再生医疗提供计划”
- 需经认可再生医疗等审查委员会审查
- 原则上不需厚生劳动省批准,但需备案
总结
日本的再生医疗等级制度体现了“风险分级、监管匹配”的原则。
第一种治疗需国家批准,厚生省组织专家审查,第二、三种需备案,但技术评审机构等级不同。
这一制度为再生医疗的临床应用提供了清晰的法律框架,也保障了患者的知情权与安全性。
在选择细胞治疗方案前,建议患者先确认治疗项目属于哪种再生医疗等级,并了解相关法规与机构资质。安全性与合规性,是再生医疗成功的关键。
参考:再生医疗法@e-Gov法令数据库